Molekylær-kinetisk teori gør det muligt, ved at analysere systemets mikroskopiske opførsel og bruge metoderne fra statistisk mekanik, at opnå vigtige makroskopiske karakteristika for det termodynamiske system. En af de mikroskopiske egenskaber, som er relateret til systemets temperatur, er den gennemsnitlige kvadratiske hastighed af gasmolekyler. Vi giver formlen for det og overvejer det i artiklen.
Ideel gas
Vi bemærker med det samme, at formlen for den kvadratiske gennemsnitshastighed af gasmolekyler vil blive givet specifikt for en ideel gas. Under det, i fysik, betragtes et sådant mange-partikelsystem, hvor partikler (atomer, molekyler) ikke interagerer med hinanden (deres kinetiske energi overstiger den potentielle interaktionsenergi med flere størrelsesordener) og ikke har dimensioner, det vil sige, at de er punkter med en endelig masse (afstanden mellem partikler, der er flere størrelsesordener større end deres størrelse.lineær).
Enhver gas, der består af kemisk neutrale molekyler eller atomer, og som er under lavt tryk og har en høj temperatur, kan betragtes som ideel. For eksempel er luft en ideel gas, men vanddamp er ikke længere sådan (stærke brintbindinger virker mellem vandmolekyler).
Molecular Kinetic Theory (MKT)

Når du studerer en ideel gas inden for rammerne af MKT, bør du være opmærksom på to vigtige processer:
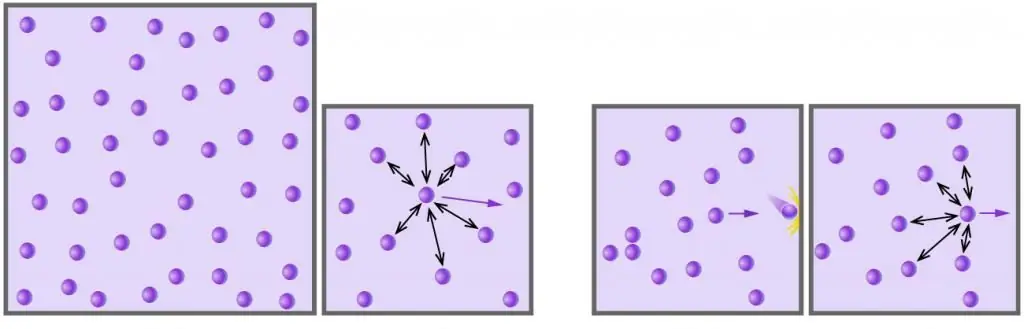
- Gas skaber tryk ved at overføre momentum, når molekyler og atomer kolliderer med dem, til væggene i det kar, der indeholder det. Sådanne kollisioner er perfekt elastiske.
- Molekyler og gasatomer bevæger sig tilfældigt i alle retninger med forskellige hastigheder, hvis fordeling adlyder Maxwell-Boltzmann-statistikker. Sandsynligheden for kollision mellem partikler er ekstremt lav på grund af deres ubetydelige størrelse og store afstande mellem dem.
På trods af at de individuelle hastigheder for gaspartikler er meget forskellige fra hinanden, forbliver gennemsnitsværdien af denne værdi konstant over tid, hvis der ikke er nogen ydre påvirkninger på systemet. Formlen for den gennemsnitlige kvadratiske hastighed af gasmolekyler kan opnås ved at overveje forholdet mellem kinetisk energi og temperatur. Vi vil behandle dette problem i artiklens næste afsnit.
Afledning af formlen for den kvadratiske gennemsnitshastighed for ideelle gasmolekyler
Enhver studerende ved fra det almindelige fysikforløb, at den kinetiske energi af translationsbevægelsen af et legeme med massen m beregnes som følger:
Ek=mv2/2
Hvor v er den lineære hastighed. På den anden side kan en partikels kinetiske energi også bestemmes ud fra den absolutte temperatur T ved hjælp af konverteringsfaktoren kB(Boltzmanns konstant). Da vores rum er tredimensionelt, beregnes Ek som følger:
Ek=3/2kBT.
Svarer til begge ligheder og udtrykker v fra dem, får vi formlen for gennemsnitshastigheden af en kvadratisk idealgas:
mv2/2=3/2kBT=>
v=√(3kBT/m).
I denne formel er m - massen af gaspartiklen. Dens værdi er ubelejlig at bruge i praktiske beregninger, da den er lille (≈ 10-27kg). For at undgå denne besvær, lad os huske den universelle gaskonstant R og den molære masse M. Konstanten R med kB er relateret af ligheden:
kB=R/NA.
Værdien af M er defineret som følger:
M=mNA.
Med hensyn til begge ligheder opnår vi følgende udtryk for molekylernes rod-middel-kvadrathastighed:
v=√(3RT/M).
Den middelkvadrathastighed af gaspartikler er således direkte proportional med kvadratroden af absolut temperatur og omvendt proportional med kvadratroden af molær masse.
Eksempel på problemløsning
Alle ved, at den luft, vi indånder, består af 99 % nitrogen og ilt. Det er nødvendigt at bestemme forskellene i gennemsnitshastighederne for molekylerne N2 og O2 ved en temperatur på 15 o C.

Dette problem vil blive løst sekventielt. Først oversætter vi temperaturen til absolutte enheder, vi har:
T=273, 15 + 15=288, 15 K.
Skriv nu molmasserne for hvert molekyle under overvejelse:
MN2=0,028 kg/mol;
MO2=0,032 kg/mol.
Da værdierne af molære masser afviger en smule, bør deres gennemsnitshastigheder ved samme temperatur også være tæt på. Ved at bruge formlen for v får vi følgende værdier for nitrogen- og oxygenmolekyler:
v (N2)=√(38, 314288, 15/0, 028)=506,6 m/s;
v (O2)=√(38, 314288, 15/0, 032)=473,9 m/s.
Fordi nitrogenmolekyler er lidt lettere end iltmolekyler, bevæger de sig hurtigere. Den gennemsnitlige hastighedsforskel er:
v (N2) - v (O2)=506,6 - 473,9=32,7 m/s.
Den resulterende værdi er kun 6,5 % af gennemsnitshastigheden for nitrogenmolekyler. Vi gør opmærksom på de høje hastigheder af molekyler i gasser, selv ved lave temperaturer.






