En gass varmekapacitet er den mængde energi, som et legeme optager, når det opvarmes med én grad. Lad os analysere hovedegenskaberne ved denne fysiske mængde.

Definitioner
En gass specifikke varme er enhedsmassen for et bestemt stof. Dens måleenheder er J/(kg·K). Mængden af varme, der absorberes af kroppen i færd med at ændre dens aggregeringstilstand, er ikke kun forbundet med start- og sluttilstanden, men også med overgangsmetoden.

afdeling
Gassernes varmekapacitet divideres med værdien bestemt ved konstant volumen (Cv), konstant tryk (Cр).
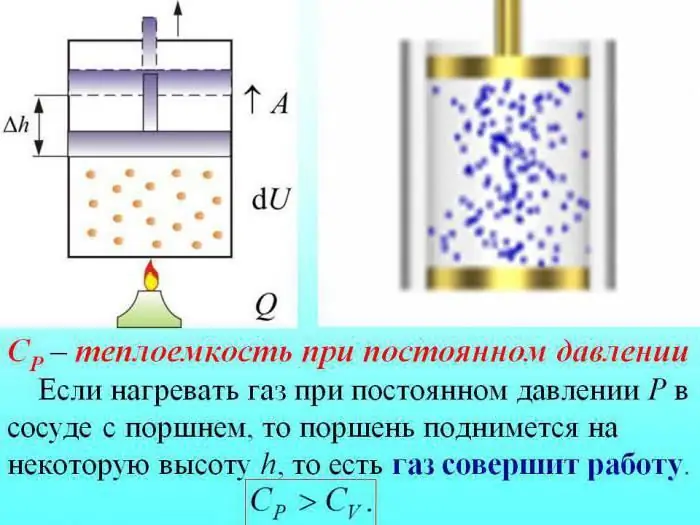
I tilfælde af opvarmning uden at ændre trykket, bruges noget varme på at producere arbejdet med gasudvidelse, og en del af energien bruges til at øge den indre energi.
Varmekapaciteten af gasser ved konstant tryk bestemmes af mængden af varme, der bruges på at øge intern energi.
Gastilstand: funktioner, beskrivelse
Varmekapaciteten af en ideel gas bestemmes under hensyntagen til, at Сp-Сv=R. Sidstnævnte størrelse kaldes den universelle gaskonstant. Dens værdi svarer til 8,314 J/(mol K).
Når man udfører teoretiske beregninger af varmekapacitet, for eksempel ved beskrivelse af forholdet til temperatur, er det ikke nok kun at bruge termodynamiske metoder, det er vigtigt at bevæbne sig med elementer af statisk fysik.
Varmekapaciteten af gasser involverer beregningen af den gennemsnitlige værdi af energien fra translationsbevægelsen af nogle molekyler. En sådan bevægelse opsummeres fra molekylets rotations- og translationsbevægelse såvel som fra atomernes indre vibrationer.
I statisk fysik er der information om, at der for hver frihedsgrad af rotations- og translationsbevægelse er en mængde for en gas, der er lig med halvdelen af den universelle gaskonstant.

Interessante fakta
En partikel af en monoatomisk gas antages at have tre translationelle frihedsgrader, så en gass specifikke varme har tre translations-, to rotations- og en vibrationsfrihedsgrader. Loven om deres ensartede fordeling fører til at ligne den specifikke varme ved et konstant volumen med R.
Under eksperimenterne blev det fundet, at varmekapaciteten af en diatomisk gas svarer til værdien R. En sådan uoverensstemmelse mellem teori og praksis forklares ved, at varmekapaciteten af en ideel gas er forbundet med kvante effekter er det derfor vigtigt, når man laver beregninger, at bruge kvantestatistikkermekanik.
Baseret på grundlaget for kvantemekanikken har ethvert system af partikler, der oscillerer eller roterer, inklusive gasmolekyler, kun nogle diskrete energiværdier.
Hvis energien fra termisk bevægelse i systemet ikke er nok til at excitere svingninger af en bestemt frekvens, bidrager sådanne bevægelser ikke til systemets samlede varmekapacitet.
Som et resultat bliver en bestemt grad af frihed "frosset", det er umuligt at anvende loven om ligedeling på den.
Gassernes varmekapacitet er en vigtig egenskab ved den tilstand, som hele det termodynamiske systems funktion afhænger af.
Den temperatur, ved hvilken loven om ekvipartition kan anvendes på vibrations- eller rotationsfrihedsgraden, er karakteriseret ved kvanteteori, forbinder Planck-konstanten med Boltzmann-konstanten.

Diatomiske gasser
Mellem mellem rotationsenerginiveauerne for sådanne gasser er et lille antal grader. Undtagelsen er brint, hvor temperaturværdien bestemmes af hundredvis af grader.
Det er grunden til, at varmekapaciteten af en gas ved konstant tryk er svær at beskrive med loven om ensartet fordeling. I kvantestatistikken tages der ved bestemmelse af varmekapaciteten i betragtning, at dens vibrationsdel, i tilfælde af et fald i temperaturen, hurtigt falder og når nul.
Dette fænomen forklarer det faktum, at der ved stuetemperatur praktisk t alt ikke er nogen vibrationsdel af varmekapaciteten, f.diatomisk gas, svarer det til konstanten R.
Varmekapaciteten af en gas ved konstant volumen i tilfælde af lavtemperaturindikatorer bestemmes ved hjælp af kvantestatistik. Der er Nernst-princippet, som kaldes termodynamikkens tredje lov. Baseret på dens formulering vil den molære varmekapacitet af en gas falde med faldende temperatur og tendere til nul.

Features of solids
Hvis varmekapaciteten af en blanding af gasser kan forklares ved hjælp af kvantestatistik, så er termisk bevægelse for en fast aggregeringstilstand karakteriseret ved små udsving af partikler nær ligevægtspositionen.
Hvert atom har tre vibrationsfrihedsgrader, og derfor kan den molære varmekapacitet af et fast stof i overensstemmelse med equipartition-loven beregnes som 3nR, hvor n er antallet af atomer i et molekyle.
I praksis er dette tal grænsen for, hvilken varmekapacitet et fast legeme har ved høje temperaturer.
Maksimum kan opnås ved almindelige temperaturer for nogle grundstoffer, herunder metaller. For n=1 er Dulong- og Petit-loven opfyldt, men for komplekse stoffer er det ret vanskeligt at nå en sådan grænse. Da grænsen ikke kan opnås i virkeligheden, sker nedbrydning eller smeltning af det faste stof.
Historie om kvanteteori
Grundlæggerne af kvanteteorien er Einstein og Debye i begyndelsen af det tyvende århundrede. Det er baseret på kvantisering af oscillerende bevægelser af atomer i en bestemtkrystal. I tilfælde af lavtemperaturindikatorer viser varmekapaciteten af et fast legeme sig at være direkte proportional med den absolutte værdi taget i terninger. Dette forhold er blevet kaldt Debyes lov. Som et kriterium, der gør det muligt at skelne mellem lav- og højtemperaturindikatorer, tages deres sammenligning med Debye-temperaturen.
Denne værdi er bestemt af spektret af vibrationer af et atom i kroppen, derfor afhænger den i høj grad af egenskaberne ved dets krystalstruktur.
QD er en værdi, der har flere hundrede K, men den er for eksempel meget højere i diamant.
Ledningselektronerne yder et væsentligt bidrag til metallers varmekapacitet. For at beregne det, bruges Fermi kvantestatistikken. Den elektroniske ledningsevne for metalatomer er direkte proportional med den absolutte temperatur. Da det er en ubetydelig værdi, tages den kun i betragtning ved temperaturer, der har tendens til det absolutte nulpunkt.
Metoder til bestemmelse af varmekapacitet
Den vigtigste eksperimentelle metode er kalorimetri. For at udføre en teoretisk beregning af varmekapaciteten anvendes statistisk termodynamik. Det er gyldigt for en ideel gas, såvel som for krystallinske legemer, udføres på grundlag af eksperimentelle data om strukturen af stof.
Empiriske metoder til at beregne varmekapaciteten af en ideel gas er baseret på ideen om den kemiske struktur, bidraget fra individuelle grupper af atomer til Ср.
For væsker anvendes også metoder, der er baseret på brugen af termodynamiskcyklusser, der gør det muligt at gå fra varmekapaciteten af en ideel gas til en væske gennem derivatet af temperaturen i fordampningsprocessens entalpi.
I tilfælde af en løsning er beregningen af varmekapaciteten som en additiv funktion ikke tilladt, da overværdien af opløsningens varmekapacitet grundlæggende er signifikant.
For at evaluere det har vi brug for den molekylær-statistiske teori om løsninger. Det sværeste er identifikation af varmekapaciteten af heterogene systemer i termodynamisk analyse.

Konklusion
Undersøgelsen af varmekapacitet giver dig mulighed for at beregne energibalancen for processer, der forekommer i kemiske reaktorer, såvel som i andre kemiske produktionsapparater. Derudover er denne værdi nødvendig for valget af optimale typer kølemidler.
På nuværende tidspunkt er den eksperimentelle bestemmelse af stoffers varmekapacitet for forskellige temperaturintervaller - fra lave værdier til høje værdier - den vigtigste mulighed for at bestemme et stofs termodynamiske egenskaber. Ved beregning af et stofs entropi og entalpi bruges varmekapacitetsintegraler. Oplysninger om varmekapaciteten af kemiske reagenser i et bestemt temperaturområde giver dig mulighed for at beregne den termiske effekt af processen. Oplysninger om løsningernes varmekapacitet gør det muligt at beregne deres termodynamiske parametre ved enhver temperaturværdi inden for det analyserede interval.
For eksempel er en væske kendetegnet ved, at en del af varmen bruges til at ændre værdien af potentiel energireagerende molekyler. Denne værdi kaldes "konfigurations"-varmekapaciteten, der bruges til at beskrive løsninger.
Det er svært at udføre fuldgyldige matematiske beregninger uden at tage hensyn til et stofs termodynamiske egenskaber, dets aggregeringstilstand. Derfor anvendes der for væsker, gasser, faste stoffer en egenskab som specifik varmekapacitet, som gør det muligt at karakterisere energiparametrene for et stof.






