Den tredimensionelle tilstand af flydende vand er svær at studere, men meget er blevet lært ved at analysere strukturen af iskrystaller. Fire tilstødende hydrogen-interagerende oxygenatomer optager hjørnerne af et tetraeder (tetra=fire, hedron=plan). Den gennemsnitlige energi, der kræves for at bryde en sådan binding i is, estimeres til 23 kJ/mol-1.

Vandmolekylers evne til at danne et givet antal brintkæder, samt en given styrke, skaber et usædvanligt højt smeltepunkt. Når det smelter, holdes det af flydende vand, hvis struktur er uregelmæssig. De fleste af hydrogenbindingerne er forvrænget. Det kræver en stor mængde energi i form af varme at bryde krystalgitteret af hydrogenbundet is.
Funktioner ved udseendet af is (Ih)
Mange af indbyggerne spekulerer på, hvilken slags krystalgitter is har. NødvendigDet skal bemærkes, at densiteten af de fleste stoffer stiger under frysning, når molekylære bevægelser bremses og tætpakkede krystaller dannes. Vandets massefylde øges også, når det afkøles til et maksimum ved 4°C (277K). Når temperaturen derefter falder under denne værdi, udvides den.
Denne stigning skyldes dannelsen af en åben, hydrogenbundet iskrystal med dens gitter og lavere tæthed, hvor hvert vandmolekyle er stift bundet af ovennævnte grundstof og fire andre værdier, mens de bevæger sig hurtigt nok til at have mere masse. Da denne handling opstår, fryser væsken fra top til bund. Dette har vigtige biologiske resultater, som et resultat af, at islaget på dammen isolerer levende væsener væk fra ekstrem kulde. Derudover er to yderligere egenskaber ved vand relateret til dets brintegenskaber: specifik varme og fordampning.
Detaljeret beskrivelse af strukturer
Det første kriterium er den mængde, der skal til for at hæve temperaturen på 1 gram af et stof med 1°C. At hæve graderne af vand kræver en relativt stor mængde varme, fordi hvert molekyle er involveret i adskillige brintbindinger, der skal brydes for at den kinetiske energi kan stige. I øvrigt betyder overfloden af H2O i celler og væv i alle store flercellede organismer, at temperaturudsving inde i cellerne minimeres. Denne funktion er afgørende, da hastigheden af de fleste biokemiske reaktionerfølsom.
Vandens fordampningsvarme er også betydeligt højere end for mange andre væsker. Der kræves en stor mængde varme for at omdanne dette legeme til en gas, fordi brintbindingerne skal brydes, for at vandmolekylerne kan forskydes fra hinanden og gå ind i den nævnte fase. Udskiftelige legemer er permanente dipoler og kan interagere med andre lignende forbindelser og dem, der ioniserer og opløses.
Andre stoffer nævnt ovenfor kan kun komme i kontakt, hvis der er polaritet. Det er denne forbindelse, der er involveret i strukturen af disse elementer. Derudover kan den rette sig rundt om disse partikler dannet af elektrolytter, så de negative oxygenatomer i vandmolekylerne er orienteret til kationerne, og de positive ioner og brintatomer er orienteret til anionerne.
I faste stoffer dannes som regel molekylære krystalgitter og atomare. Det vil sige, at hvis jod er bygget på en sådan måde, at det indeholder I2, , så er CO2 molekyler i fast kuldioxid, dvs. i tøris. placeret ved krystalgitterknuderne . Når is interagerer med lignende stoffer, har is et ionisk krystalgitter. Grafit, for eksempel, som har en atomstruktur baseret på kulstof, er ikke i stand til at ændre det, ligesom diamant.
Hvad sker der, når en krystal af bords alt opløses i vand: polære molekyler tiltrækkes af ladede elementer i krystallen, hvilket fører til dannelsen af lignende partikler af natrium og klorid på overfladen, hvilket resulterer i disse legemerer forskudt fra hinanden, og det begynder at opløses. Herfra kan det observeres, at is har et krystalgitter med ionbinding. Hvert opløst Na + tiltrækker de negative ender af flere vandmolekyler, mens hver opløst Cl - tiltrækker de positive ender. Skallen, der omgiver hver ion, kaldes flugtkuglen og indeholder norm alt flere lag af opløsningsmiddelpartikler.
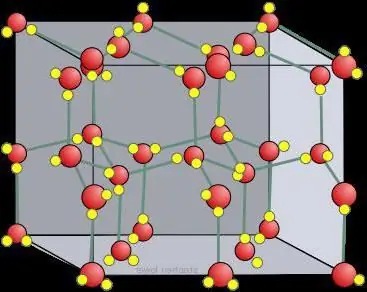
Tøriskrystalgitter
Variabler eller en ion omgivet af grundstoffer siges at være sulfateret. Når opløsningsmidlet er vand, hydreres sådanne partikler. Ethvert polært molekyle har således en tendens til at blive solvatiseret af elementerne i det flydende legeme. I tøris danner typen af krystalgitter atombindinger i aggregeringstilstanden, som er uændrede. En anden ting er krystallinsk is (frosset vand). Ioniske organiske forbindelser såsom carboxylase og protonerede aminer skal være opløselige i hydroxyl- og carbonylgrupper. Partiklerne i sådanne strukturer bevæger sig mellem molekyler, og deres polære systemer danner hydrogenbindinger med denne krop.
Selvfølgelig påvirker antallet af de sidst angivne grupper i et molekyle dets opløselighed, hvilket også afhænger af reaktionen af forskellige strukturer i grundstoffet: for eksempel er en-, to- og tre-carbonalkoholer blandbare med vand, men større kulbrinter med enkelte hydroxylforbindelser er meget mindre fortyndede i væsker.
Hexagonal Ih ligner i formenatomisk krystalgitter. For is og al naturlig sne på Jorden ser det præcis sådan ud. Dette fremgår af symmetrien af krystalgitteret af is, dyrket fra vanddamp (det vil sige snefnug). Den er i rumgruppe P 63/mm fra 194; D 6h, Laue klasse 6/mm; svarende til β-, som har et multiplum af 6 spiralakse (rotation rundt foruden forskydning langs den). Den har en ret åben lavdensitetsstruktur, hvor effektiviteten er lav (~1/3) sammenlignet med simple kubiske (~1/2) eller frontcentrerede kubiske (~3/4) strukturer.
Sammenlignet med almindelig is er krystalgitteret af tøris, bundet af CO2-molekyler, statisk og ændrer sig kun, når atomer henfalder.
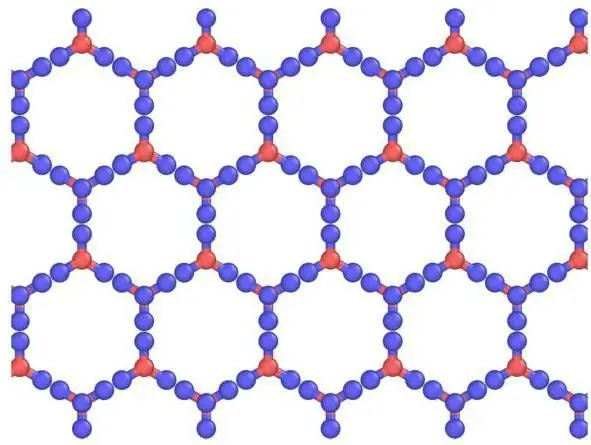
Beskrivelse af gitre og deres elementer
Krystaller kan ses som krystallinske modeller, der består af plader placeret over hinanden. Hydrogenbindingen er ordnet, mens den i virkeligheden er tilfældig, da protoner kan bevæge sig mellem vand(is)molekyler ved temperaturer over omkring 5 K. Det er sandsynligt, at protoner opfører sig som en kvantevæske i en konstant tunnelstrøm. Dette forstærkes af spredningen af neutroner, der viser deres spredningstæthed halvvejs mellem oxygenatomerne, hvilket indikerer lokalisering og samordnet bevægelse. Her er der en lighed mellem is og et atomært, molekylært krystalgitter.
Molekyler har et forskudt arrangement af brintkædenmed hensyn til sine tre naboer i flyet. Det fjerde element har et formørket hydrogenbindingsarrangement. Der er en lille afvigelse fra perfekt hexagonal symmetri, da enhedscellen er 0,3 % kortere i denne kædes retning. Alle molekyler oplever de samme molekylære miljøer. Der er nok plads inde i hver "kasse" til at indeholde partikler af interstitielt vand. Selvom de ikke generelt betragtes, er de for nylig blevet detekteret effektivt ved neutrondiffraktion af isens pulverformige krystalgitter.
Ændring af stoffer
Det sekskantede legeme har tredobbelte punkter med flydende og gasformigt vand 0,01 ° C, 612 Pa, faste elementer - tre -21,985 ° C, 209,9 MPa, elleve og to -199,8 ° C, 70 MPa, samt - 34,7 °C, 212,9 MPa. Den dielektriske konstant for sekskantet is er 97,5.
Smeltekurven for dette grundstof er givet ved MPa. Tilstandsligningerne er tilgængelige, ud over dem, nogle simple uligheder, der relaterer ændringen i fysiske egenskaber til temperaturen af sekskantet is og dens vandige suspensioner. Hårdhed svinger med grader, der stiger fra eller under gips (≦2) ved 0°C til feldspat (6 Mohs) ved -80°C, en unorm alt stor ændring i absolut hårdhed (> 24 gange).
Det sekskantede krystalgitter af is danner sekskantede plader og søjler, hvor de øvre og nedre flader er basalplanerne {0 0 0 1} med en entalpi på 5,57 μJ cm -2, og andre tilsvarende sidedele kaldes dele af prismet {1 0 -1 0} med 5, 94µJ cm -2. Sekundære overflader {1 1 -2 0} med 6,90 ΜJ ˣ cm -2 kan dannes langs planerne dannet af strukturernes sider.
En sådan struktur viser et unorm alt fald i termisk ledningsevne med stigende tryk (såvel som kubisk og amorf is med lav tæthed), men adskiller sig fra de fleste krystaller. Dette skyldes en ændring i hydrogenbindingen, som reducerer lydens tværgående hastighed i krystalgitteret af is og vand.
Der er metoder, der beskriver, hvordan man forbereder store krystalprøver og enhver ønsket isoverflade. Det antages, at hydrogenbindingen på overfladen af det sekskantede legeme, der undersøges, vil være mere ordnet end inde i bulksystemet. Variationsspektroskopi med fase-gitterfrekvensgenerering har vist, at der er en strukturel asymmetri mellem de to øverste lag (L1 og L2) i den underjordiske HO-kæde af den basale overflade af hexagonal is. De vedtagne hydrogenbindinger i de øvre lag af sekskanterne (L1 O ··· HO L2) er stærkere end dem, der accepteres i det andet lag til den øvre akkumulering (L1 OH ··· O L2). Interaktive sekskantede isstrukturer tilgængelige.
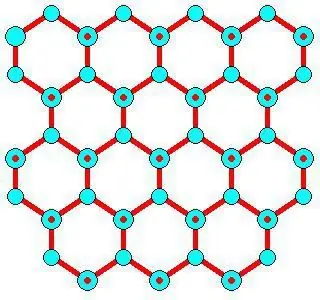
Udviklingsfunktioner
Det mindste antal vandmolekyler, der er nødvendige for at danne is, er cirka 275 ± 25, som for en komplet icosahedral klynge på 280. Dannelse sker med en hastighed på 10 10 ved luft-vand-grænseflade og ikke i bulkvand. Væksten af iskrystaller afhænger af forskellige væksthastigheder af forskelligeenergier. Vand skal beskyttes mod frysning, når biologiske prøver, fødevarer og organer frysekonserveres.
Dette opnås typisk ved hurtige afkølingshastigheder, brug af små prøver og en kryokonservator og øget tryk for at danne is og forhindre celleskade. Den frie energi af is/væske stiger fra ~30 mJ/m2 ved atmosfærisk tryk til 40 mJ/m-2 ved 200 MPa, hvilket indikerer grunden til, at denne effekt opstår.
Hvilken type krystalgitter er karakteristisk for is
Alternativt kan de vokse hurtigere fra prismeoverflader (S2) på den tilfældigt forstyrrede overflade af lynfrosne eller ophidsede søer. Væksten fra {1 1 -2 0}-fladerne er mindst den samme, men gør dem til prismebaser. Dataene om udviklingen af iskrystallen er blevet fuldt undersøgt. De relative væksthastigheder af elementer af forskellige ansigter afhænger af evnen til at danne en stor grad af ledhydrering. Temperaturen (lav) af det omgivende vand bestemmer graden af forgrening i iskrystallen. Partikelvækst er begrænset af diffusionshastigheden ved en lav grad af underafkøling, dvs. <2 °C, hvilket resulterer i flere af dem.

Men begrænset af udviklingskinetik ved højere niveauer af depression på >4°C, hvilket resulterer i nålevækst. Denne form ligner strukturen af tøris (har et krystalgitter med en sekskantet struktur), forskelligekarakteristika for overfladeudvikling og temperaturen af det omgivende (superkølede) vand, som ligger bag snefnugs flade former.
Danningen af is i atmosfæren påvirker i høj grad skyernes dannelse og egenskaber. Feltspat, der findes i ørkenstøv, der kommer ind i atmosfæren i millioner af tons om året, er vigtige former. Computersimuleringer har vist, at dette skyldes kernedannelsen af prismatiske iskrystalplaner på overfladeplaner med høj energi.
Nogle andre elementer og gitter
Opløste stoffer (med undtagelse af meget lille helium og brint, som kan trænge ind i mellemrummene) kan ikke indgå i Ih-strukturen ved atmosfærisk tryk, men presses ud til overfladen eller det amorfe lag mellem partiklerne i mikrokrystallinsk krop. Der er nogle andre elementer på gitterstederne for tøris: kaotrope ioner såsom NH4 + og Cl -, som indgår i lettere væskefrysning end andre kosmotrope, såsom Na + og SO42-, så det er ikke muligt at fjerne dem på grund af det faktum, at de danner en tynd film af den resterende væske mellem krystallerne. Dette kan føre til elektrisk opladning af overfladen på grund af dissociation af overfladevand, der balancerer de resterende ladninger (hvilket også kan føre til magnetisk stråling) og en ændring i pH af de resterende væskefilm, fx NH 42SO4 bliver mere surt, og NaCl bliver mere basisk.
De er vinkelrette på ansigternekrystalgitter af is, der viser det næste lag vedhæftet (med O-atomer i sort). De er karakteriseret ved en langsomt voksende basal overflade {0 0 0 1}, hvor kun isolerede vandmolekyler er knyttet. En hurtigt voksende {1 0 -1 0} overflade af et prisme, hvor par af nytilknyttede partikler kan binde sig til hinanden med brint (en brintbinding/to molekyler af et grundstof). Det hurtigst voksende ansigt er {1 1 -2 0} (sekundær prismatisk), hvor kæder af nyligt vedhæftede partikler kan interagere med hinanden ved hydrogenbinding. Et af hendes kæder/elementmolekyle er en form, der danner kamme, der deler sig og tilskynder til transformation til to sider af prismet.
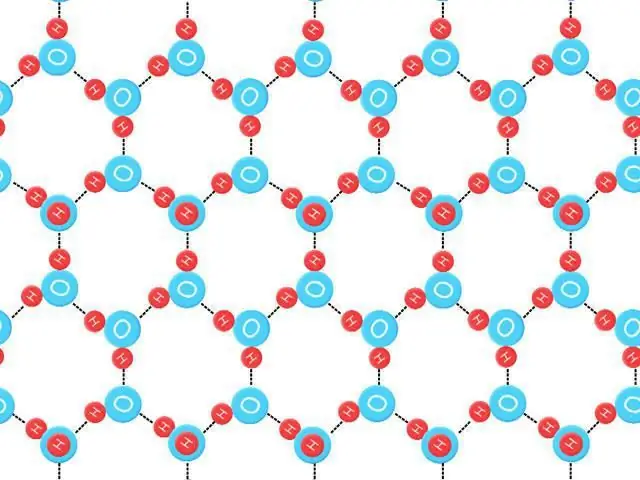
Nulpunktsentropi
Kan defineres som S 0=k B ˣ Ln (N E0), hvor k B er Boltzmann-konstanten, NE er antallet af konfigurationer ved energien E, og E0 er den laveste energi. Denne værdi for entropien af hexagonal is ved nul Kelvin overtræder ikke termodynamikkens tredje lov "Entropien af en ideel krystal ved absolut nul er nøjagtig nul", da disse grundstoffer og partikler ikke er ideelle, har uordnet hydrogenbinding.
I denne krop er hydrogenbindingen tilfældig og skifter hurtigt. Disse strukturer er ikke helt lige i energi, men strækker sig til et meget stort antal energisk tætte tilstande, adlyder "isens regler". Nulpunktsentropi er den lidelse, der ville forblive, selvom materialet kunne afkøles til absolutnul (0 K=-273, 15 °C). Genererer eksperimentel forvirring for hexagonal is 3, 41 (± 0, 2) ˣ mol -1 ˣ K -1. Teoretisk set ville det være muligt at beregne nul-entropien af kendte iskrystaller med meget større nøjagtighed (forsømmer defekter og energiniveauspredning) end at bestemme den eksperimentelt.
Forskere og deres arbejde på dette område
Kan defineres som S 0=k B ˣ Ln (N E0), hvor k B er Boltzmann-konstanten, NE er antallet af konfigurationer ved energien E, og E0 er den laveste energi. Denne værdi for entropien af hexagonal is ved nul Kelvin overtræder ikke termodynamikkens tredje lov "Entropien af en ideel krystal ved absolut nul er nøjagtig nul", da disse grundstoffer og partikler ikke er ideelle, har uordnet hydrogenbinding.
I denne krop er hydrogenbindingen tilfældig og skifter hurtigt. Disse strukturer er ikke helt lige i energi, men strækker sig til et meget stort antal energisk tætte tilstande, adlyder "isens regler". Nulpunktsentropi er den uorden, der ville forblive, selvom materialet kunne afkøles til det absolutte nulpunkt (0 K=-273,15°C). Genererer eksperimentel forvirring for hexagonal is 3, 41 (± 0, 2) ˣ mol -1 ˣ K -1. Teoretisk set ville det være muligt at beregne nul-entropien af kendte iskrystaller med meget større nøjagtighed (forsømmer defekter og energiniveauspredning) end at bestemme den eksperimentelt.

Selvom rækkefølgen af protoner i bulk-is ikke er ordnet, foretrækker overfladen sandsynligvis rækkefølgen af disse partikler i form af bånd af hængende H-atomer og O-enkeltpar (nul entropi med ordnede hydrogenbindinger). Nulpunktsforstyrrelsen ZPE, J ˣ mol -1 ˣ K -1 og andre findes. Ud fra alt det ovenstående er det klart og forståeligt, hvilke typer krystalgitre der er karakteristiske for is.






