I vores tid er fysik blevet en meget almindelig videnskab. Det er bogstaveligt t alt til stede over alt. Det mest elementære eksempel: et æbletræ vokser i din have, og frugter modnes på det, tiden kommer, og æblerne begynder at falde, men i hvilken retning falder de? Takket være loven om universel gravitation falder vores foster til jorden, det vil sige, det går ned, men ikke op. Det var et af de mest berømte eksempler på fysik, men lad os være opmærksomme på termodynamik eller mere præcist faseligevægte, som ikke er mindre vigtige i vores liv.
Termodynamik

Først og fremmest, lad os se på dette udtryk. ΘερΜοδυναΜική - sådan ser ordet ud på græsk. Den første del ΘερΜo betyder "varme", og den anden δυναΜική betyder "styrke". Termodynamik er en gren af fysikken, der studerer egenskaberne ved et makroskopisk system, samt forskellige måder at omdanne og overføre energi på. I dette afsnit er forskellige tilstande og processer specielt undersøgt, så begrebet temperatur kan introduceres i beskrivelsen (dette er en fysisk størrelse, der kendetegner et termodynamisk system og måles vha.visse apparater). Alle igangværende processer i termodynamiske systemer beskrives kun af mikroskopiske størrelser (tryk og temperatur, samt koncentrationen af komponenter).
Clapeyron-Clausius-ligning
Alle fysikere kender denne ligning, men lad os bryde den ned stykke for stykke. Det refererer til ligevægtsprocesserne for overgangen af bestemt stof fra en fase til en anden. Dette ses tydeligt i sådanne eksempler: smeltning, fordampning, sublimering (en af måderne at konservere produkter på, hvilket foregår ved fuldstændig at fjerne fugt). Formlen viser tydeligt de igangværende processer:
- n=PV/RT;
- hvor T er stoffets temperatur;
- P-tryk;
- R-specifik faseovergangsvarme;
- V-ændring i specifik volumen.
Historien om oprettelsen af ligningen

Clausius-Clapeyron-ligningen er en fremragende matematisk forklaring på termodynamikkens anden lov. Også omt alt som "Clausius-uligheden". Naturligvis blev sætningen udviklet af videnskabsmanden selv, som ønskede at forklare sammenhængen mellem varmestrømmen i systemet og entropien samt dets miljø. Denne ligning blev udviklet af Clausius i hans forsøg på at forklare og kvantificere entropi. I bogstavelig forstand giver sætningen os mulighed for at afgøre, om en cyklisk proces er reversibel eller irreversibel. Denne ulighed giver os en kvantitativ formel til at forstå den anden lov.
Forskeren var en af de første, der arbejdede på ideen om entropi, og gav den enddaprocesnavn. Det, der nu er kendt som Clausius' sætning, blev først offentliggjort i 1862 i Rudolfs sjette værk, On the Use of the Transformation Equivalence Theorem for Interior Work. Videnskabsmanden forsøgte at vise et proportion alt forhold mellem entropi og energiflow ved opvarmning (δ Q) i systemet. I byggeriet kan denne termiske energi omdannes til arbejde, og den kan omdannes til varme gennem en cyklisk proces. Rudolph beviste, at "den algebraiske sum af alle transformationer, der forekommer i en cyklisk proces, kun kan være mindre end nul eller, i ekstreme tilfælde, lig med nul."
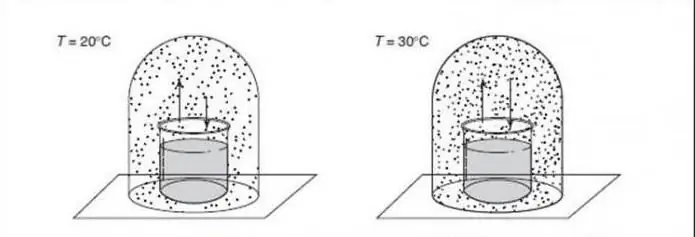
Lukket isoleret system
Isoleret system er et af følgende:
- Det fysiske system er langt fra andre, der ikke interagerer med dem.
- Det termodynamiske system er lukket af stive, ubevægelige vægge, hvorigennem hverken stof eller energi kan passere.
På trods af det faktum, at emnet er internt relateret til sin egen tyngdekraft, tages et isoleret system norm alt ud over grænserne for ydre tyngdekraft og andre fjerne kræfter.
Dette kan sammenlignes med det, der (i den mere generelle terminologi brugt i termodynamik) kaldes et lukket system omgivet af selektive vægge, hvorigennem energi kan overføres i form af varme eller arbejde, men ikke stof. Og med et åbent system, hvor stof og energi kommer ind eller ud, selvom det kan have forskellige uigennemtrængelige vægge idele af dens grænser.
Et isoleret system adlyder fredningsloven. Oftest i termodynamik betragtes stof og energi som separate begreber.
Termodynamiske overgange
For at forstå kvantefaseovergange er det nyttigt at sammenligne dem med klassiske transformationer (også kaldet termiske inversioner). CPT beskriver spidsen i et systems termodynamiske egenskaber. Det signalerer omorganiseringen af partikler. Et typisk eksempel er den frysende overgang af vand, som beskriver en glidende overgang mellem en væske og et fast stof. Klassiske fasevækster skyldes konkurrencen mellem systemets energi og entropien af dets termiske fluktuationer.
Et klassisk system har ingen entropi ved nultemperatur, og der kan derfor ikke forekomme fasetransformation. Deres rækkefølge er bestemt af det første diskontinuerlige afledte termodynamiske potentiale. Og selvfølgelig har den den første ordre. Fasetransformationer fra en ferromagnet til en paramagnet er kontinuerlige og anden orden. Disse konstante ændringer fra en ordnet til en uordnet fase er beskrevet af en ordensparameter, der er nul. For ovennævnte ferromagnetiske transformation vil ordreparameteren være den totale magnetisering af systemet.
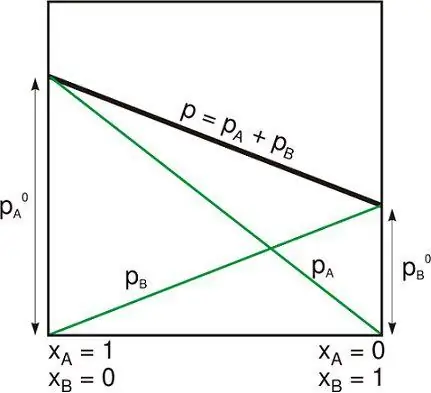
Gibbs potentiale
Gibbs Free Energy er den maksimale mængde arbejde uden ekspansion, der kan fjernes fra et termodynamisk lukket system (der kan udveksle varme og arbejde med miljøet). Sådandet maksimale resultat kan kun opnås i en fuldstændig reversibel proces. Når systemet transformerer tilbage fra den første tilstand til den anden, er reduktionen i Gibbs frie energi lig med den, der udføres af systemet i dets omgivelser, minus trykkræfternes arbejde.
Saldostater

Termodynamisk og mekanisk ligevægt er et aksiomatisk begreb inden for termodynamik. Dette er den indre tilstand af et eller flere systemer, der er forbundet med mere eller mindre permeable eller uigennemtrængelige vægge. I denne tilstand er der ingen rene makroskopiske strømme af stof eller energi, hverken i et system eller mellem systemer.
I sin egen opfattelse af tilstanden af indre ligevægt forekommer makroskopiske ændringer ikke. Systemerne er samtidigt i gensidig termisk, mekanisk, kemisk (konstant), strålingsligevægt. De kan være i samme form. I denne proces gemmes alle visninger på én gang og på ubestemt tid, indtil den fysiske drift er brudt. I makroskopisk ligevægt finder helt præcise afbalancerede udvekslinger sted. Ovenstående bevis er en fysisk forklaring på dette koncept.
Grundlæggende
Hver love, sætninger, formler har deres eget grundlag. Lad os se på de 3 grundlag for loven om faseligevægt.
- Fase er en form for stof, homogen i kemisk sammensætning, fysisk tilstand og mekanisk balance. Typiske faser er faste, flydende og gasformige. To ikke-blandbare væsker (eller flydende blandinger med forskellige sammensætninger) adskilt af en separat grænse betragtes som to adskilte faser og ikke-blandbare faste stoffer.
- Antallet af komponenter (C) er antallet af kemisk uafhængige komponenter i systemet. Det mindste antal uafhængige arter, der kræves for at bestemme sammensætningen af alle faser af systemet.
- Antallet af frihedsgrader (F) i denne sammenhæng er antallet af intensive variabler, der er uafhængige af hinanden.
Klassificering efter faseligevægt
- Reaktioner af kontinuerlig nettooverførsel (ofte kaldet faststofreaktioner) forekommer mellem fast stof af forskellig sammensætning. De kan omfatte grundstoffer, der findes i væsker (H, C), men disse grundstoffer tilbageholdes i faste faser, så ingen flydende faser er involveret som reaktanter eller produkter (H2O, CO2). Faste rene overføringsreaktioner kan være kontinuerlige eller diskontinuerlige eller terminale.
- Polymorfe er en speciel type fastfasereaktion, der inkluderer faser med identisk sammensætning. Klassiske eksempler er reaktionerne mellem aluminiumsilikater kyanit-sillimanit-andalusit, omdannelsen af grafit til diamant ved højt tryk og ligevægten af calciumcarbonat.
Love of Equilibrium

The Gibbs Factory Rule blev foreslået af Josiah Willard Gibbs i hans berømte papir med titlen "The Equilibrium of Heterogeneous Substances", som udkom fra 1875 til 1878. Det gælder forikke-reaktive multikomponent heterogene systemer i termodynamisk ligevægt og er en given lighed:
- F=C-P+2;
- hvor F er antallet af frihedsgrader;
- C – antal komponenter;
- P - antal faser i termodynamisk ligevægt med hinanden.
Antallet af frihedsgrader er antallet af ubesatte intensive variabler. Det største antal termodynamiske parametre, såsom temperatur eller tryk, der kan variere samtidigt og vilkårligt uden at påvirke hinanden. Et eksempel på et en-komponent system er et med et enkelt rent kemikalie, mens to-komponent systemer, såsom blandinger af vand og ethanol, har to uafhængige komponenter. Typiske faseovergange (faseligevægt) er faste stoffer, væsker, gasser.
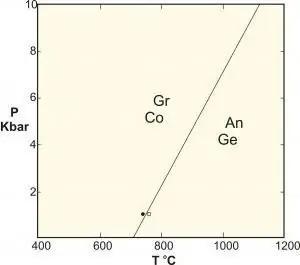
Faseregel ved konstant tryk
For anvendelser inden for materialevidenskab, der beskæftiger sig med faseskift mellem forskellige faste strukturer, opstår der ofte et konstant tryk (f.eks. én atmosfære) og ignoreres som en frihedsgrad, så reglen bliver: F=C - P + 1.
Denne formel introduceres nogle gange under navnet "reglen for kondenseret fase", men som vi ved, er den ikke anvendelig for disse systemer, der er udsat for høje tryk (f.eks. i geologi), da konsekvenserne af disse pres kan forårsage katastrofale konsekvenser.
Det kan virke som om faseligevægt bare er en tom sætning, og der er få fysiske processer, hvor dette øjebliker involveret, men som vi har set, uden det, virker mange af de love, vi kender, ikke, så du skal sætte dig lidt ind i disse unikke, farverige, omend lidt kedelige regler. Denne viden har hjulpet mange mennesker. De lærte at anvende dem på sig selv, for eksempel kan elektrikere, der kender reglerne for arbejde med faser, beskytte sig mod unødvendig fare.

