Ideel gas, den ideelle gasligning for tilstand, dens temperatur og tryk, volumen… listen over parametre og definitioner, der bruges i det tilsvarende afsnit af fysik, kan fortsættes i ret lang tid. I dag vil vi kun tale om dette emne.
Hvad betragtes i molekylær fysik?

Hovedobjektet, der overvejes i dette afsnit, er en ideel gas. Den ideelle gasligning for tilstand blev opnået under hensyntagen til normale miljøforhold, og vi vil tale om dette lidt senere. Lad os nu nærme os dette "problem" på afstand.
Lad os sige, at vi har en masse gas. Dens tilstand kan bestemmes ved hjælp af tre parametre af termodynamisk karakter. Disse er naturligvis tryk, volumen og temperatur. Ligningen for systemets tilstand vil i dette tilfælde være formlen for forholdet mellem de tilsvarende parametre. Det ser sådan ud: F (p, V, T)=0.
Her nærmer vi os for første gang langsomt fremkomsten af sådan noget som idealgas. Det kaldes en gas, hvor interaktionerne mellem molekyler er ubetydelige. Generelt findes dette ikke i naturen. Men enhver meget forkælet gas er tæt på den. Nitrogen, ilt og luft, som er under normale forhold, adskiller sig lidt fra idealet. For at skrive tilstandsligningen for en ideel gas kan vi bruge den forenede gaslov. Vi får: pV/T=const.
Relateret koncept 1: Avogadros lov
Han kan fortælle os, at hvis vi tager det samme antal mol af absolut enhver tilfældig gas og sætter dem under de samme forhold, inklusive temperatur og tryk, så vil gasserne optage det samme volumen. Især blev forsøget udført under normale forhold. Det betyder, at temperaturen var 273,15 Kelvin, trykket var én atmosfære (760 millimeter kviksølv eller 101325 Pascal). Med disse parametre optog gassen et volumen svarende til 22,4 liter. Derfor kan vi sige, at for et mol af enhver gas vil forholdet mellem numeriske parametre være en konstant værdi. Derfor blev det besluttet at betegne denne figur med bogstavet R og kalde det den universelle gaskonstant. Det er således lig med 8,31. Enheden er J/molK.
Ideel gas. Den ideelle gasligning for tilstand og dens manipulation
Lad os prøve at omskrive formlen. For at gøre dette skriver vi det i denne form: pV=RT. Dernæst udfører vi en simpel handling, multiplicerer begge sider af ligningen med et vilkårligt antal mol. Vi får pVu=uRT. Lad os tage højde for det faktum, at produktet af det molære volumen ogmængden af stof er simpelthen volumen. Men når alt kommer til alt, vil antallet af mol samtidig være lig med kvotienten af massen og den molære masse. Sådan ser Mendeleev-Clapeyron-ligningen ud. Det giver en klar idé om, hvilken slags system en ideel gas danner. Tilstandsligningen for en ideel gas vil have formen: pV=mRT/M.
Udled formlen for tryk
Lad os lave nogle flere manipulationer med de opnåede udtryk. For at gøre dette multipliceres højre side af Mendeleev-Clapeyron-ligningen og divideres med Avogadro-tallet. Nu ser vi omhyggeligt på produktet af mængden af stof ved Avogadro-tallet. Dette er intet andet end det samlede antal molekyler i gassen. Men på samme tid vil forholdet mellem den universelle gaskonstant og Avogadro-tallet være lig med Boltzmann-konstanten. Derfor kan formler for tryk skrives som følger: p=NkT/V eller p=nkT. Her er symbolet n partikelkoncentrationen.
Ideelle gasprocesser
I molekylær fysik er der sådan noget som isoprocesser. Det er termodynamiske processer, der finder sted i systemet ved en af de konstante parametre. I dette tilfælde skal stoffets masse også forblive konstant. Lad os se mere specifikt på dem. Så lovene for en ideel gas.
Presset forbliver konstant
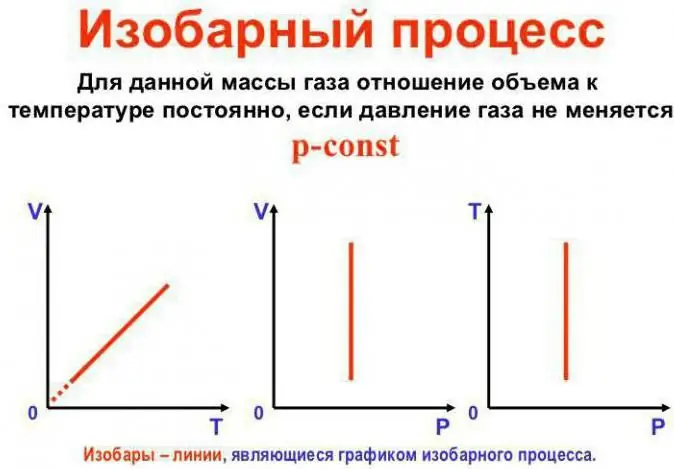
Dette er Gay-Lussacs lov. Det ser sådan ud: V/T=konst. Det kan omskrives på en anden måde: V=Vo (1 + at). Her er a lig med 1/273,15 K^-1 og kaldes "volumenudvidelseskoefficienten". Vi kan erstatte temperaturen i både Celsius ogKelvin-skalaen. I sidstnævnte tilfælde får vi formlen V=Voat.
Lydstyrken forbliver konstant

Dette er Gay-Lussacs anden lov, mere almindeligt omt alt som Charles' lov. Det ser sådan ud: p/T=konst. Der er en anden formulering: p=po (1 + at). Transformationer kan udføres i overensstemmelse med det foregående eksempel. Som du kan se, minder de ideelle gaslove nogle gange ret meget om hinanden.
Temperaturen forbliver konstant

Hvis temperaturen af en ideel gas forbliver konstant, så kan vi få Boyle-Mariotte-loven. Det kan skrives sådan: pV=const.
Relateret koncept 2: Delvis pres
Lad os sige, at vi har et fartøj med gasser. Det bliver en blanding. Systemet er i en tilstand af termisk ligevægt, og gasserne reagerer ikke med hinanden. Her vil N betegne det samlede antal molekyler. N1, N2 og så videre, henholdsvis antallet af molekyler i hver af komponenterne i blandingen. Lad os tage trykformlen p=nkT=NkT/V. Den kan åbnes for en specifik sag. For en to-komponent blanding vil formlen have formen: p=(N1 + N2) kT/V. Men så viser det sig, at det samlede tryk vil blive summeret ud fra parti altrykket for hver blanding. Så det vil se ud som p1 + p2 og så videre. Disse vil være delpressene.
Hvad er det til?
Formlen, vi fik, indikerer, at trykket i systemet er fra hver gruppe af molekyler. Det afhænger i øvrigt ikke afandre. D alton udnyttede dette, da han formulerede loven, senere opkaldt efter ham: i en blanding, hvor gasser ikke kemisk reagerer med hinanden, vil det samlede tryk være lig med summen af parti altrykkene.






